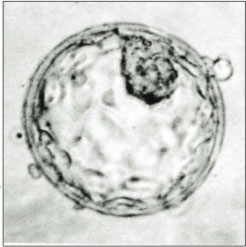
Ludzka blastula, blastocysta; Mr. J. Conaghan; domena publiczna; wikipedia
Początek poematu cesarza Hadriana,
Animula, vagula, blandula
Hospes comesque corporis
w kanonicznym w Polsce tłumaczeniu Kazimierza Morawskiego brzmi:
Duszyczko moja, tkliwa, ruchliwa,
Gościu ty ciała mojego i druhno
Choć powstały rozliczne (także i polskie) tłumaczenia pożegnalnego wiersza Hadriana, dość jasno pobrzmiewa w nich wszystkich niepokój i troska – dokąd to pobłądzi uchodząca z cesarza duszyczka (W jakie ty strony odejdziesz bladziutka, naga, zziębnięta?, zapytuje w swym tłumaczeniu Zygmunt Kubiak)? Jakie będą jej dalsze losy?
Pośmiertne losy Hadriana nie będą tematem dzisiejszej notki, tym bardziej, że to raczej mitologiczna niźli medyczna kwestia, jednak błądząca cesarska duszyczka może przywoływać nie tylko skojarzenia natury – powiedzmy – schyłkowej. I tu możemy już spojrzeć na rzecz w sposób bliższy codziennej perspektywie patologów. Niebagatelną wszak kwestią jest przecież także ta, dokąd trafi nasza metaforyczna duszyczka na początku swej drogi i gdzie się zagnieździ. Bo też i losy zapłodnionej komórki jajowej nie są – jak zapewne pamiętacie – wcale tak oczywiste, jak mogłoby się w pierwszej chwili wydawać. Wiemy że efekty zapłodnienia bywają niekiedy różne, niekoniecznie zbliżone do tych zazwyczaj oczekiwanych. Podobnie bywa z docelową lokalizacją zarodka tudzież zarodków wskutek zapłodnienia powstałych.

Urzęsiony nabłonek wyściełający ścianę jajowodu; http://www.siumed.edu/~dking2/index.htm via Davidson College, davidson.edu
Plemniki, mknąc z zawrotną prędkością rzędu 100 mikrometrów na sekundę, docierają zazwyczaj do komórki jajowej w bańce jajowodu (najdłuższej i najszerszej jego części), po czym to rozpoczyna się wieloetapowy i wielogodzinny proces, który zbiorczo określamy mianem zapłodnienia. Jego rezultat, czyli najpierw zygota, a z biegiem kolejnych godzin i dni odpowiednio – przypominająca owoc morwy morula, później zaś pęcherzykowata blastula, czyli blastocysta, powoli przemieszcza się w stronę miejsca, gdzie docelowo zagnieździ się, by spokojnie dalej rozwijać się i rosnąć. Standardowo dzięki ruchom perystaltycznym (robaczkowym, jak w przewodzie pokarmowym) mięśniówki jajowodu i ruchom rzęsek nabłonka wyściełającego ścianę tego narządu zarodek około 3-4 dnia rozwoju powinien dotrzeć do jamy macicy, a pięcio-sześciodniowa blastocysta powinna zacząć się mościć wygodnie w odpowiednio do tego celu przygotowanym dzięki wpływom hormonalnym endometrium, błonie śluzowej jamy macicy, nadtrawiając jego składowe i powoli zagłębiając się, tak iż 11-12 dnia rozwoju w miejscu wniknięcia zarodka pozostaje jedynie znaczący jego ślad skrzep (zagnieżdżaniu, czyli implantacji, może towarzyszyć przejściowe krwawienie zwane implantacyjnym). Tak rzecz powinna wyglądać w sytuacji modelowej i tak zazwyczaj, jeśli ciąża ma przebiegać prawidłowo, wygląda. Ale przecież nie zawsze wszystko idzie tak, jak powinno.

Ciąża jajowodowa; jajowód usunięty operacyjnie i rozcięty, by uwidocznić zarodek i zaczątki łożyska; CDC/Dr. Edwin P. Ewing, Jr., domena publiczna
Ściślej mówiąc – coś idzie nie tak w mniej więcej jednym do dwóch na sto przypadków ciąż obserwowalnych klinicznie (pomińmy wszystkie te sytuacje, w których zarodek obumarł zanim ktokolwiek zauważył jego pojawienie się). Czasami zarodek z różnych względów nie dociera w pożądane miejsce i zagnieżdża się gdzie indziej. Przyczyny mogą być różne. W wielu przypadkach trudno je jednoznacznie wskazać. Pośród głównych podejrzanych na pewno znajdziemy wszelkie czynniki zmieniające strukturę jajowodów – czy to wcześniejsze zabiegi chirurgiczne, czy stany zapalne chociażby. Taki pechowy zarodek w pechowym jajowodzie może po prostu pozostać, nie przemieszczając się dalej w stronę jamy macicy i rzeczywiście znakomita większość – ponad 95% – ciąż ektopowych (pozamacicznych) to właśnie ciąże jajowodowe. Może też nasza blastula vagula pobłądzić w kierunku jajnika (do 3% przypadków) lub hen, hen, daleko, by osiąść gdzieś w jamie brzusznej (ok. 1-2% błędnych duszyczek), ewentualnie skromniej – zaczepić się gdzieś bliziutko na zewnątrz w okolicy macicy (np. w obrębie aparatu więzadłowego podtrzymującego narząd), tudzież – zupełnie odwrotnie – podążywszy dalej i dotarłszy do jamy macicy, nie zdołać – na przykład ze względu na zrosty pooperacyjne czy pozapalne – “zapuścić korzeni” na czas i w odpowiednim miejscu, i powędrować do kanału szyjki macicy, by ostatecznie zagnieździć się w ścianie szyjki (mniej niż 1%).

Ciąża pozamaciczna; R. de Graaf, De Mulierum Organis Generationi Inservientibus, reprint z listu Benoit Vassala do Royal Society, 1669; domena publiczna
W jajowodzie najczęściej zarodek pozostaje tam, gdzie i najczęściej dochodzi do zapłodnienia – w bańce (ok. 80% ciąż jajowodowych), choć może przemieścić się w stronę jajnika, bądź zbliżyć do leżącej bliżej macicy cieśni jajowodu, czy nawet (na szczęście rzadko, taka sytuacja może bowiem skończyć się pęknięciem ściany macicy) utknąć w śródściennej jego części przebiegającej – zgodnie z nazwą – już w obrębie mięśniówki ściany macicy (ciąża jajowodowa śródścienna zwana też rogową, od lokalizacji – rogu macicy).

Lewostronna ciąża jajowodowa; czerwone strzałki pokazują rozdęty, nabrzmiały krwistą treścią jajowód, niebieskie – trzon macicy; Mikael Häggström; CC BY-SA 3.0

Macica z prawostronną ciążą jajowodową, koniec 3 miesiąca rozwoju; C- rozerwany jajowód, E- płód; A nurse’s handbook of obstetrics, 1915; https://www.flickr.com/photos/internetarchivebookimages/14782335102/
Tak, jak uczyniłaby to w jamie macicy, tu również blastocysta zaczyna się zagnieżdżać. Jej część rozwijająca się w kierunku tkanek łożyskowych, trofoblast, powoli nadtrawia ścianę jajowodu, kosmki stopniowo naciekają warstwę mięśniową i surowicówkę, światło samego jajowodu poszerza się, wypełniając krwią i tkankami łożyskowymi, choć tkanki ciężarnej w tym miejscu nigdy nie przejdą w pełni przemian tworzących funkcjonalne podłoże dla przyszłego łożyska, jakie w prawidłowo rozwijających się ciążach wytwarza śluzówka jamy macicy. Zazwyczaj całemu procesowi towarzyszy różnie nasilony odczyn zapalny. Jeśli takie rozwijające się jajo płodowe nie obumrze i nie zostanie przez organizm spontanicznie wchłonięte (tak, to się zdarza), jeśli nie zostanie równie spontanicznie wydalone (niekiedy do jamy brzusznej zresztą poprzez lejek jajowodu – mówimy wtedy o poronieniu jajowodowym), cóż – będzie rosło. A, pamiętajmy, jajowód to nie jama macicy, nie ma szans, by poszerzył się na tyle, by pozwolić na pełen rozwój płodowy, jego ściana zaś jest zbyt cienka i anatomicznie słabo przystosowana do rozwoju łożyska. Jajowód będzie się poszerzał, jego ściana będzie coraz cieńsza i coraz bardziej rozciągnięta, aż – zazwyczaj około ósmego tygodnia rozwoju – w końcu po prostu pęknie. Jedna czwarta takich rozdętych “zaciążonych” jajowodów ulegnie rozerwaniu zanim lekarze zdążą zorientować się w stanie pacjentki. Krwotok towarzyszący pęknięciu jajowodu bywa masywny, niejednokrotnie z fatalnymi dla kobiety skutkami – ciąża pozamaciczna to nadal jeden z istotnych czynników zabijających ciężarne (według różnych źródeł stanowi nawet do kilkunastu procent przyczyn zgonów), a pośród czynników zabijających je w pierwszym trymestrze jest przyczyną wiodącą.

Ciżą jajowodowa – przekrój; zaznaczone miejsce rozerwania, gdzie naciekające kosmki tworzącego się łożyska znacząco osłabiły ścianę narządu; Obstetrics for nurses, 1922; https://www.flickr.com/photos/internetarchivebookimages/14766416075/
Aktualne wytyczne postępowania w przypadku ciąży jajowodowej obejmują – zależnie od parametrów klinicznych (m.in. poziom gonadotropiny kosmówkowej pozwalający ocenić przebieg ciąży, stopień poszerzenia jajowodu, stan ogólny pacjentki) – interwencję chirurgiczną bądź farmakologiczną, ewentualnie – w przypadku ściśle wyselekcjonowanych pacjentek, u których można podejrzewać, że dojdzie do samoistnego obumarcia zarodka – postawę wyczekującą (choć tu zaleca się dużą ostrożność).

Ciąża jajowodowa może niekiedy okazać się ciążą bliźniaczą; http://ispub.com/IJGO/16/2/14212#
Interwencja chirurgiczna jest niezbędna w przypadku już pękniętej ciąży pozamacicznej, jednak ma zastosowanie także u pacjentek “stabilnych”. Przebieg procedury zasadniczo jest dość prosty – należy usunąć przyczynę dolegliwości tudzież zagrożenie dla chorej. Poza usunięciem całego jajowodu (salpingektomia) istnieje, oczywiście, też możliwość przeprowadzenia zabiegu oszczędzającego z linijnym nacięciem jajowodu (salpingotomia) i usunięciem jego zawartości, co intuicyjnie wydawałoby się zwiększać szanse pacjentki na kolejną ciążę (jakkolwiek badania wydają się tych intuicji nie potwierdzać). W przypadku sporego odsetka ciąż jajowodowych preferowaną metodą jest opcja farmakologiczna zakończenia ciąży, czyli metotreksat pozwalający uniknąć zabiegu chirurgicznego.

Stanowisko polskich teologów w kwestii ciąż ektopowych bywa różne – http://teologiamoralna.pl/wp-content/uploads/2013/01/Kraj.pdf
Dobór optymalnego w danym przypadku postępowania – podkreślę ponownie – zależy od sytuacji klinicznej. A dlaczego podkreślam? Bo niekiedy pomiędzy parametry kliniczne wkrada się ideologia. Pół biedy jeśli jest to ideologia kierująca pacjentką – dorośli, świadomi swej sytuacji, nieubezwłasnowolnieni pacjenci mają prawo odmówić zalecanej terapii. Niestety, zdarza się, że czynnikiem wpływającym na przebieg leczenia jest ideologia z góry narzucana przez gremia zarządzające daną placówką medyczną, a względy ideologiczne niekoniecznie stawiają na pierwszym miejscu dobro pacjentki. Tymczasem nieodpowiednio potraktowana ciąża jajowodowa może zabić. Zarodka, zauważę złośliwie, raczej to nie uratuje.
Złośliwości na bok jednak. Czy taki zagnieżdżony w jajowodzie zarodek ma jakieś szanse? Cóż, póki przebywa w jajowodzie – nie. Nasuwający się być może niektórym w pierwszej chwili pomysł – “to go wyjmijmy” – nie znalazł szerszego zastosowania w praktyce klinicznej. Owszem, archiwa medyczne przechowują zapisy pojedynczych prób przeniesienia go do jamy macicy, o wartości raczej anegdotycznej i trudnej do zweryfikowania, mamy jednak zarówno podstawy merytoryczne (byłaby to wysoce inwazyjna procedura wymagająca doskonałego zgrania czasowego – tak by wczesny, na czas wykryty zarodek dał radę zagnieździć się w przewidywanym dlań prawidłowym miejscu), jak i wzmianki o nieudanych eksperymentach wystarczające, by nie traktować podobnego pomysłu ze szczególną rewerencją (choć badać podobne możliwości zapewne warto). Ale jest przecież inny sposób opuszczenia ciasnych ścian jajowodu. Tak, nieco dramatyczny.

Ten płód również “zaczepił się” na zewnętrznej ścianie macicy, obumarł ok. 23 tygodnia rozwoju; CC-BY; http://www.ncbi.nlm.nih.gov/pmc/articles/PMC4397520/
Krwotok towarzyszący rozerwaniu jajowodu bywa bardzo groźny. Rzecz może się skończyć wstrząsem i śmiercią pacjentki. Zarodek niemal zawsze przy okazji ginie. Ale zdarzają się zupełnie pojedyncze przypadki, gdy krwawienie ulega samoograniczeniu, a zarodek, wypłynąwszy na zewnątrz, przyczepia się do jakiegoś bardziej niźli jajowód wytrzymałego obiektu – na przykład zewnętrznej ściany macicy. To nie są tak komfortowe warunku do rozwoju, jak te zapewniane przez jamę macicy, ale już dają jakieś szanse przeżycia (podkreślmy – szanse, to że zarodek zaimplantuje się w nowym miejscu, wcale jeszcze nie oznacza, że jego historia zakończy się pozytywnie). Tyle że to trochę jak z wygraną na loterii – fajnie, jeśli się przydarzy, ale zazwyczaj na to nie liczymy, zaciągając kredyt, a jeśli już koniecznie chcemy podjąć takie ryzyko, lepiej by była to nasza własna decyzja, a nie zewnętrzny przymus.

Śródoperacyjne zdjęcie przedstawiające zlokalizowany na podstawnej powierzchni prawego płata wątroby worek owodniowy; CC-BY; http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3519057/
W przytłaczającej większości przypadków lokalizacja jajowodowa to dla zarodka wyrok śmierci. Los bywa nieco łaskawszy dla tych nielicznych embrionów, które pobłądziły nieco dalej. Ciąże brzuszne to rzadkość, jednak zasięg rażenia mają zaiste imponujący. Taki zarodek potrafi się zagnieździć w każdym właściwie miejscu, do którego zdoła dotrzeć – i może to być zarówno wątroba, jak i ściana pęcherza moczowego czy jelita, ale też śledziona (naprawdę – dobrze czytacie, śledziona), sieć, powierzchnia przepony czy ściany jamy brzusznej. Część takich ciąż – nazywanych wtórnymi – to efekt sytuacji takiej jak wyżej opisana – pierwotnie jajowodowa ciąża ektopowa, która rozerwała jajowód, nie dając objawów wystarczających, by zaalarmować pacjentkę i zarodek, który miał dość szczęścia, by podczas tego incydentu nie obumrzeć i znaleźć sobie nowy punkt zaczepienia, część to przypadki poronień jajowodowych. Pierwotne ciąże brzuszne to duszyczki, które pobłądziły bez prób implantacji w jajowodzie – od razu zagnieżdżając się gdzieś w obrębie jamy brzusznej.

Łożysko przyczepione częściowo do ściany zewnętrznej macicy, częściowo do ściany jelita (w dłoni po lewej), pośrodku – pępowina; http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3158531/
Niezależnie od swego pierwotnego czy wtórnego pochodzenia pozamaciczne ciąże brzuszne udaje się (choć rzadko, często zresztą niechcący, wskutek zbyt późnego zarejestrowania lokalizacji płodu) doprowadzić do etapu, na którym możliwy jest przy współpracy chirurgów happy end. Choć i one same, i próby ich usunięcia wiążą się z zagrożeniem życia i zdrowia ciężarnej (od rozerwanej śledziony po zgon z wykrwawienia) z ryzykiem zgonu sięgającym 20%, choć te wczesne nader często obumierają samoistnie, a ze względu na niebagatelne jednak ryzyko zazwyczaj jednak – przy odpowiednio wczesnej diagnozie – podobne ciąże się terminuje, te bardziej zaawansowane poddaje się niejednokrotnie ostrożnej obserwacji (przy późnej ciąży brzusznej próba jej usunięcia może być dla ciężarnej bardziej niebezpieczna niż kontynuacja ciąży), doprowadzając przy dużej dozie szczęścia do donoszenia zdrowego dziecka. I to jest potencjalnie znakomita wiadomość dla niektórych pacjentek – pod warunkiem, że nikt nie będzie na nich wymuszał bohaterstwa i narażania zdrowia i życia celem utrzymania takiej ciąży.
A jeśli uważacie, że ciąża brzuszna jest zjawiskiem spektakularnym u człowieka, może powinniście zwrócić uwagę na inne gatunki. Bo też, jak się zapewne domyślacie, nie są ciąże ektopowe bynajmniej patologią ograniczoną do H. sapiens, choć specyfika ludzkich ciąż pozamacicznych może być od innych gatunków odmienna, chociażby ze względu na różną anatomię i fizjologię narządu rodnego, np. ciąże jajowodowe u zwierząt innych niż naczelne nie są częste, dużo częściej obserwuje się wtórne ciąże brzuszne wywołane uszkodzeniem ściany macicy “wyrzucającym” zarodki/płody na zewnątrz, co przy ciążach mnogich u niektórych gatunków może dawać dość dramatyczny efekt. No ale to już temat na inny artykuł.

Ciąża brzuszna u samicy królika związana z pęknięciem lewego rogu macicy (strzałka); https://rep.bioscientifica.com/view/journals/rep/131/4/1310631.xml
(Przypominam tylko, że patologów możecie śledzić też na fejsbuku – warto tam zaglądać)
Literatura:
Blausteins Pathology of the Female Genital Tract. J Kurman, L Hedrick Ellenson, BM Ronnett, 6th ed. 2011
Ciąża ektopowa. G Jakiel, D Robak-Chołubek, J Tkaczuk-Włach; Przegląd Menopauzalny 2006;1:61–64
Diagnostyka i leczenie ciąży ektopowej. M Sobstyl, J Tkaczuk-Włach, W Bednarek, G Jakiel; Przegląd Menopauzalny 2012;5:431–435
Does This Woman Have an Ectopic Pregnancy? The Rational Clinical Examination Systematic Review. JR Crochet, LA Bastian, MV Chireau; Journal of the Americam Medical Association 2013;309(16):1722-1729
Ectopic pregnancy in animals and humans. JM Corpa; Reproduction 2006;131:631-40
Conservative management of tubal ectopic pregnancy. NM van Mello, F Mol, BW Mol, PJ Hajenius; Best Practice & Research. Clinical Obstetrics and Gynaecology 2009;23(4):509-18
Surgical treatment of ectopic pregnancy. M Agdi, T Tulandi; Best Practice & Research. Clinical Obstetrics and Gynaecology 2009;23(4):519–527
Treating non-tubal ectopic pregnancy. M Chetty, J Elson; Best Practice & Research. Clinical Obstetrics and Gynaecology 2009;23(4):529-38
Management of extra-tubal and rare ectopic pregnancies: case series and review of current literature. R Oliver, M Malik, A Coker, J Morris; Archives of Gynecology and Obstetrics 2007;276(2): 125-131
Diagnosing ectopic pregnancy and current concepts in the management of pregnancy of unknown location. E Kirk, C Bottomley, T Bourne; Human Reproduction Update 2014;20(2):250-61
Ectopic pregnancy in uncommon implantation sites. S Badr, AN Ghareep, LM Abdulla, R Hassanein; The Egyptian Journal of Radiology and Nuclear Medicine 2013;44(1):121-30
Unilateral Tubal Twin Ectopic Pregnancy: An Unusual Case. A Kakani, S Goel, D Shrivastava, V Shrivastava; The Internet Journal of Gynecology and Obstetrics; 16(2)
Extra-uterine twin pregnancy: case report of spontaneous bilateral tubal ectopic pregnancy. BH Amine, S Haythem; The Pan African Medical Journal 2015;20:435
Spontaneous Unruptured Bilateral Tubal Pregnancy: A Case Report. N Ghomian, M Lotfalizadeh; Iranian Journal of Medical Sciences 2015;40(6):537-40
Ruptured ectopic pregnancy presenting as intestinal obstruction. S Singh, BK Jain, D Mohanty, J Agrawal, S Mehta; Canadian Journal of Surgery 2009;52(4):E99–E100
Primary hepatic pregnancy. R Yadav, C Raghunandan, S Agarwal, S Dhingra, S Chowdhary; Journal of Emergency, Trauma, and Shock 2012;5(4):367–369
Hepatic Pregnancy Suspected at Term and Successful Delivery of a Live Neonate With Placental Attachment to the Right Lobe of the Liver. KJ Brouard, BR Howard, RA Dyer; Obstetrics and Gynecology 2015;126(1):207-10
An Early Abdominal Wall Ectopic Pregnancy Successfully Treated with Ultrasound Guided Intralesional Methotrexate: A Case Report. PM Anderson, EK Opfer, JM Busch, EF Magann; Obstetrics and Gynecology International 2009;Article ID 247452
Primary abdominal ectopic pregnancy: a case report. R Yildizhan, A Kolusari, F Adali, E Adali, M Kurdoglu, C Ozgokce, N Cim; Cases Journal 2009;2:8485
Hemoperitoneum in advanced abdominal pregnancy with a live baby: a case report. D Matovelo, N Ng’walida; BMC Research Notes 2014;7:106
Secondary abdominal pregnancy in urinary bladder. OP Sharma; Gynaecology and Obstetrics Imaging 2006;16(4):815-818
Do Religious Restrictions Influence Ectopic Pregnancy Management? A National Qualitative Study. AM Foster, A Dennis, F Smith; Women’s Health Issues 2011;21(2):104-9


Pingback: Przystawki – czyli 6 blogonotek naukowych do poczytania | NeuroBigos
Zgroza mnie bierze po przeczytaniu komentarza ks. prof. dr hab….
LikeLike
Pingback: Z życia autystki: o chodzeniu na protesty i aborcji - Pisarka na spektrum